工业合成氨
合成氨的反应原理
1.加热试管中的铁丝绒至红热后注入氢气和氨气的混合气体,可以看到湿润的PH试纸变蓝色
2.用氢 气和氨气合成氨的反应式是
 ,属放热反应。
,属放热反应。
3.工业上,采用以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件下合成氨。
(1)催化剂的主要作用:成千上万倍地加快化学反应速率,缩短达平衡的时间,提高日产量。
(2)合成氨的适宜条件:以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件
(3)选择适宜生产条件的原则:有较高的反应速率和平衡转化率,能最大限度地提高利润。
(4)合成氨生产时,不采用尽可能高的压强,通常采用10MPa~30MPa 的压强,否则会增大设备的动力要求,增大成本。
(5)合成氨的反应为放热反应,降低温度促使平衡向有移动,有利于N2、H2转化为NH3;但降温必然减缓了反应速率,影响单位时间产率。生产中将二者综合考虑,既要保证N2、H2的转化率,又要保证较快的反应速率,只能选择适中的温度400~500℃左右。应注意该温度为催化剂活化温度,低于此温度,催化剂不起作用。
(6)催化剂是影响反应速率的几个因素中,对反应速率影响程度最大的。
催化剂的特点:
①选择性:不 同的反应选择不同的催化剂,如合成氨选择了铁触媒。每种催化剂都是对特定的反应有催化作用,并非能改变任何化学反应的速率。
②灵敏性:催化剂中混入杂质,常常会失去催化作 用,称催化剂“中毒”,因此 反应气体进入反应器前必须净化。 ③催化剂只有在活化温度以上才能起催化作用,如铁触媒活化温度为400~500℃,因此该温度为合成氨的适宜温度。
合成氨
合成氨:
1.生产原理

2.合成氨的基本生产过程
(1)原料气的制备要实现合成氨的工业化生产,首先要解决氢气和氮气的来源问题。
①氮气的制备合成氨所需要的氮气都取自空气。从空气中制取氮气通常有两种方法:一是将空气液化后蒸发分离出氧气而获得氮气;二是将空气中的氧气与碳作用生成二氧化碳,再除去二氧化碳得到氮气。
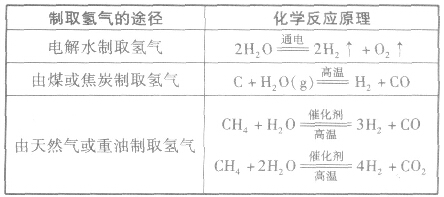
②氢气的制备氢气主要来源于水和碳氢化合物。氢气的制取有下表中的几条途径。
(2)原料气的净化
原料气的净化就是除去原料气中的杂质。在制取原料气的过程中,常混有一些杂质,其中的某些杂质会使合成氨所用的催化剂“中毒”(所谓“中毒”即是催化剂失去催化活性),所以必须除去。原料气净化的主要目的是防止催化剂“中毒”。
(3)氨的合成与分离
①氨的合成工业合成氨的主要设备是合成塔。将净化后的原料气经过压缩机压缩后输人合成塔,经过下列化学反应合成氨:

②氨的分离从合成塔出来的混合气体,通常约含15%(体积分数)的氨。为了使氨从未反应的氮气和氢气里分离出来,要把混合气体通过冷凝器使氨液化,然后在气体分离器里把液态氨分离出来导入液氨贮罐。南气体分离器出来的气体,经过循环压缩机,再送到合成塔中进行反应。
3.合成氨适宜条件的选择
外加条件要尽可能加快反应速率,提高反应物的转化率.

4.合成氨的环境保护
随着环境保护意识的增强,以及相关的法律、法规的严格实施,合成氨生产中可能产生的“三废”的处理越来越成为技术改造的重要问题。
(1)废渣
主要来自造气阶段,特别是以煤为原料而产生的煤渣,用重油为原料产生的炭黑等,现在大都将它们用作建材和肥料的原料。
(2)废气
主要是H2S和CO2等气体。对H2S气体的处理,先后采用了直接氧化法(选择性催化氧化)、循环法(使用溶剂将其吸收浓缩)等回收技术。对CO2 的处理,正在不断研究和改进将其作为尿素和碳铵生产原料的途径。
(3)废液
主要是含氰化物和含氨的污水。目前,处理含氰化物污水主要有生化、加压水解、氧化分解、化学沉淀、反吹回炉等方法;处理含氨废水多以蒸馏的方法回收氨达到综合利用的目的,对浓度过低的含氨废水,可用离子交换法治理。
合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂,氨在平衡混合物中的含量仍较少。最近英国俄勒冈大学的化学家使用了一种名为trans一Fe(DMeOPrPE)2的新催化剂,在常温下合成氨,反应方程式可表示为
N2+3H2 2NH3。有关说法正确的是
2NH3。有关说法正确的是 [ ] A.哈伯法合成氨是吸热反应,新法合成氨是放热反应
B.新法合成氨不需要在高温条件下,可节约大量能源,具有发展前景
C.新法合成氨能在常温下进行是因为不需要断裂化学键
D.新催化剂降低了反应所需要的能量,提高了活化分子百分数下列反应起了氮的固定作用的是 [ ] A.N2与H2在一定条件下反应生成NH3
B.由NH3制碳铵和硫铵等化肥
C.NH3经催化氧化生成NO
D.NO与O2反应生成NO2下列反应属于氮的固定的是 [ ] ①N2和H2在一定条件下反应生成NH3
②雷雨闪电时空气中的N2和O2化合生成NO
③NH3经过催化氧化生成NO
④NH3和HNO3反应生成NH4NO3
A.①③
B.②④
C.③④
D.①②起固定氮作用的化学反应是 [ ] A.N2与H2在一定条件下反应生成NH3
B.硝酸工厂用NH3氧化制NO
C.雷雨时空气中的N2转化为NO
D.由NH3制碳酸氢铵和硫酸铵工业上合成氨的原料之一--氢气,有一种来源是取自石油气,例如烷烃。根据以上叙述,回答下列问题
(1)有人设计了以下反应途径,假设反应都能进行,你认为最合理的是[ ] A. 
B.
C.
D.
(2)按以上最合理的反应途径,理论上用1mol丙烷可制得氨 [ ] A.4mol
B.6.7mol
C.10 mol
D.2.7mol(3)该合理的反应途径最显著的优点是 [ ] A.简单易行
B.制得的H2纯度高
C.制取H2的产量高
D.可同时获得大量热能工业合成氨与制备硝酸一般可连续生产,流程如下 
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)  CO2+H2
CO2+H2
①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=__________(填计算结果)。
②保持温度不变,向上述平衡体系中再加入0.1molCO,当反应重新建立平衡时,水蒸气的转化率
α(H2O)=________。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中 T1____573K(填“>”、“<”或“=”)。 
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:4NH3(g)+5O2(g)  4NO(g)+6H2O(g) △H=
4NO(g)+6H2O(g) △H=
-905kJ·mol-1 不同温度下NO产率如图所示。温度高于900℃时, NO产率下降的原因______________。
(4)废水中的N、P元素是造成水体富营养化的关键因素,农药厂排放的废水中常含有较多的NH4+和
PO43-,一般可以通过两种方法将其除去。
①方法一:将Ca(OH)2或CaO 投加到待处理的废水中,生成磷酸钙,从而进行回收。当处理后的废水中
c(Ca2+)=2×10-7mol/L时,溶液中c(PO43-)=____________mol/L。(已知Ksp[Ca3(PO4)2]=2×10-33)
②方法二:在废水中加入镁矿工业废水,就可以生成高品位的磷矿石―鸟粪石,反应的方程式为
Mg2++NH4++PO43-=MgNH4PO4↓。该方法中需要控制污水的pH为7.5~10,若pH高于10.7,鸟粪石的产量会大大降低。其原因可能为________________________________________。与方法一相比,方法二的优点为___________________________。氨气在农业和国防工业都有很重要的作用,历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气合成氨的化学家。
(1)下图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答
对于合成氨的反应下列说法正确的是_____________(填编号)。
A.该反应在任意条件下都可以自发进行
B.加入催化剂,能使该反应的E和△H都减小
C.若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1>K2
D.该反应属于人工固氮
(2)现在普遍应用的工业合成氨的方法为N2+3H2 2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。
2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是_________________。
A.使用的更高效催化剂
B.升高温度
C.及时分离出氨气
D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2L的密闭容器中发生N2+3H2 2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=_______________。从11min起,压缩容器的体积为
2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=_______________。从11min起,压缩容器的体积为
1L,则n(N2)的变化曲线为_____________________。
A. a B.b C.c D.d
(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通人一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质里,用吸附在它内外表面上的金属钯多晶薄膜作电极,实现了常压、570℃条件下高转化率的电解法合成氮(装置如右上图)。则钯电极上的电极反应式是_____________________________。 下列反应起了氮的固定作用的是 [ ] A.NH3经催化氧化获得NO
B.NO2跟水作用制取硝酸
C.NH3+CO2+H2O=NH4HCO3
D.N2+O2=2NO(放电条件)德国人弗里茨·哈伯(Fritz Haber)由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是 [ ] A.N2和H2在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.由氨制取硝酸过程中,氮元素被还原下列有关合成氨工业的说法中,正确的是 [ ] A.生产中常使用某种廉价易得的原料适当过量,以提高另一原料的转化率
B.合成氨的反应是放热的,所以合成氨时温度越低,对氨的工业生产越有利
C.合成氨工业的温度控制在500℃,目的是使化学平衡向正反应方向移动
D.合成氨厂采用的压强是20MPa~50MPa,是因为该压强下铁触媒的活性最大(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨的原理是:  △H <0,生产流程如图所示。
△H <0,生产流程如图所示。 
①X的化学式为____________;
②上图中条件选定的主要原因是(选填字母序号)______________;
A.升高温度、增大压强均有利于氨的合成
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③ 改变反应条件,会使平衡发生移动。下图表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是(选填字母序号)______________,当横坐标为温度时,变化趋势正确的是(选填字母序号)______________。
(2)某温度下体积为200L的氨合成塔中,测得如下数据 
根据表中数据计算0~2小时内N2的平均反应速率______________mol·L-1·h-1若起始时与平衡时的压强之比为a,则N2的转化率为______________(用含a的代数式表示)若C3=1.200 mol·L-1,则该条件下反应
2NH3(g) N2(g)+3H2(g)的平衡常数______________。
N2(g)+3H2(g)的平衡常数______________。
(3)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水且显弱碱性的过程:________________;
②氨水中水电离出的c(OH-)_______10-7 mol·L-1(填写“>”、“<”或“=”);
③将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到小依次为___________。科学家一直致力于研究常温.常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照.N2压力1.0×105 Pa.反应时间3 h): 
相应的热化学方程式如下: N2(g)+3H2O(1)==2NH3(g)+ O2(g) △H1=+765.2 kJ·mol-1
回答下列问题:
(1)请在下边的坐标图中,画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:________________________________________________ 。 (3)工业合成氨的反应为N2(g)+3H2(g)  2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为。计算
2NH3(g)。设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60molH2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为。计算
①该条件下N2的平衡转化率;
②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。 关于氨的合成工业的下列说法正确的是 [ ] A.从合成塔出来的气体,其中氨气一般占15%,所以生产氨的工业的效率都很低
B.由于NH3易液化,N2、H2可循环使用,则总的说来氨的产率很高
C.合成氨工业的反应温度控制在400~500 ℃左右,目的是使平衡向正反应方向进行
D.合成氨工业采用10 MPa ~ 30MPa ,是因该条件下催化剂的活性最好工业合成氨的反应是在500℃左右进行,主要原因是 [ ] A.500℃时反应速率最快
B.500℃时氨气的平衡浓度最大
C.500℃时反应物的转化率最高
D.500℃时催化剂能发挥最大效力合成氨的温度和压强通常控制在约500℃以及200~500atm的范围,且进入合成塔的N2和H2的体积比为1:3,经科学测定,在相应条件下,N2和H2反应所得氨的平衡浓度(体积分数)如下表所示。而实际从合成塔出来的混合气体中含有氨约为15%,这表明 
[ ] A.表中所测数据有明显误差
B.生产条件控制不当
C.氨的分解速率大于预测值
D.合成塔中的反应并未达平衡氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为N2+3H2 2NH3,则在电化学合成氨的过程中,阳极反应式为________________,阴极反应式为______________。
2NH3,则在电化学合成氨的过程中,阳极反应式为________________,阴极反应式为______________。
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g) △H<0,其化学平衡常数K与t的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与t的关系如下表: 
①试确定K1的相对大小,K1____________ 4.1×106(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是____________ (填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.2v(N2)(正) = v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是____________ 。
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为___________
A.[Cl-]>[NH4+]>[H+]>[OH-]
B.[NH4+]>[Cl-]>[OH-]>[H+]
C.[Cl-]>[NH4+]>[OH-]>[H+]
D.[NH4+]>[Cl-]>[H+]>[OH-]氨是重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国化学家哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)  2NH3(g);△H=-92.4 kJ/mol,他因此获得了1918年度诺贝尔化学奖。试回答下列问题:
2NH3(g);△H=-92.4 kJ/mol,他因此获得了1918年度诺贝尔化学奖。试回答下列问题:
⑴ 下列方法不适合实验室制取氨气的是_____________(填序号)。
A.向生石灰中滴入浓氨水
B.加热浓氨水
C.直接用氢气和氮气合成
D.向饱和氯化铵溶液中滴入浓氢氧化钠溶液
⑵ 合成氨工业中采取的下列措施可用勒夏特列原理解释的是_______________(填序号)。
A.采用较高压强(20 MPa~50 MPa)
B.采用500℃的高温
C.用铁触媒作催化剂
D.将生成的氨液化并及时从体系中分离出来,未反应的N2和H2循环到合成塔中
(3) 用数字化信息系统DIS(如下图Ⅰ所示:它由传感器、数据采集器和计算机组成)可以测定上述氨水的浓度。用酸式滴定管准确量取0.5000 mol/L醋酸溶液25.00 mL于烧杯中,以该种氨水进行滴定,计算机屏幕上显示出溶液导电能力随氨水体积变化的曲线如下图Ⅱ所示。
①用滴定管盛氨水前,滴定管要用_____________润洗2~3遍,
②试计算该种氨水的浓度:________________。
③下列情况下,会导致实验结果c(NH3·H2O)偏低的是____________。
A.滴定结束时仰视读数
B.量取25.00 mL醋酸溶液时,未用所盛溶液润洗滴定管
C.滴定时,因不慎将氨水滴在烧杯外
(4)1998年希腊亚里士多德大学的Marnellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨。其实验装置如下图。
正极的电极反应式为:_______________________________。 过渡元素在生活、生产和科技等方面有广泛的用途。
⑴应用于合成氨反应的催化剂(铁)的表面上存在氮原子,下图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则图示铁颗粒表面上氮原子与铁原子的个数比为
_________________。
⑵现代污水处理工艺中常利用聚合铁{简称PFS,化学式为: [Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是______________ 。(填序号)
A.PFS中铁显+3价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
⑶铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅲ)与甲基丙烯酸根的配合物为 
①该化合物中存在的化学键类型有______________。
②该化合物中一个Cr的配位数为______________。
③甲基丙烯酸分子中C原子的杂化方式有______________。
④等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是______________。(填一种即可)
⑤与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是____________。(填元素符号)合成氨工业对国民经济和社会发展具有重要的意义。合成塔中发生反应为:N2(g)+3H2(g)  2NH3(g) △H<0
2NH3(g) △H<0
(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g) CO2(g)+H2(g) △H>0 ①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K =_______________________。②保持温度不变,向上述平衡体系中再加入0.1mol CO,当反应重新建立平衡时,水蒸气的总转化率α (H2O)_______________________。
CO2(g)+H2(g) △H>0 ①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K =_______________________。②保持温度不变,向上述平衡体系中再加入0.1mol CO,当反应重新建立平衡时,水蒸气的总转化率α (H2O)_______________________。
(2)下表为不同温度下合成氨反应的平衡常数。由表可推知T1_______573K(填“>”、“<”或“=”)。
(3)673K,30MPa下n(NH3) 和n(H2) 随时间变化的关系如下图所示依据上图,下列有关叙述正确的是(填写序号)__________________。
A.c点表示n(NH3)和n(H2)相等
B.c点表示NH3生成速率与NH3分解速率相同
C.e点和d点时反应的平衡常数相同
D.c点时正反应速率大于逆反应速率
(4)用NO2溶于水制硝酸:3NO2+H2O  2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因用化学平衡移动的理论进行解释是_________________________________。
2HNO3+NO。从生产流程看,吸收塔中需要补充空气,其原因用化学平衡移动的理论进行解释是_________________________________。
(5)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ·mol-1 CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ·mol-1 则甲烷直接将NO2还原为N2的热化学方程式为:______________________________。下列说法正确的是 [ ] A.塑料袋、废纸、橡胶制品均属于有机物制品
B.合成氨工业与接触法制硫酸中SO2催化氧化的过程都采用了高压的生产条件
C.在医院中为酸中毒病人输液应采用0.9%氯化铵溶液
D.夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏原因,并打开所有门窗通风工业合成氨与制备硝酸一般可连续生产,流程如下 
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g)  CO2+H2。t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=________(填计算结果)。
CO2+H2。t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=________(填计算结果)。
(2)合成培中发生反应N2(g)+3H2(g) 2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1_______300℃(填“>”、“<”或“=”)。
2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1_______300℃(填“>”、“<”或“=”)。 
(3)N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示。温度高于900℃时,NH3产率下降的原因_________________。 
(4)在上述流程图中,氧化炉中发生反应的化学方程式为_____________________。
(5)硝酸厂的尾气含有氮的氧化物,如果不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g)△H= -574kJ·mol-1
CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H= -1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:_________________。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式______________,科学家利用此原理,设计成氨气--氧气燃料电池,则通入氨气的电极是________(填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为___________________。合成氨工业的主要反应为:N2(g) +3H2(g)  2NH3(g) △H<0,下图是合成氨的简要流程示意图
2NH3(g) △H<0,下图是合成氨的简要流程示意图

(1)写出设备A、B的名称:A________,B________;沿X路线进入压缩机的物质是________。
(2)原料气往往混有CO、NH3等杂质,在进入合成塔之前需净化,净化的原因是________。
(3)氮、氢混合气体送入合成塔前要通过压缩机压缩的原因是________________;在合成塔中及时分离出氨气的目的是________________。
(4)工业合成氨的反应为:N2(g) + 3H2(g) 2NH3(g) △H<0,当压强为30MPa,温度为500℃时,在容积为1L的密闭容器中充入1molN2和3molH2,反应达到平衡时NH3的体积分数为20%,求此时的平衡常数________。
2NH3(g) △H<0,当压强为30MPa,温度为500℃时,在容积为1L的密闭容器中充入1molN2和3molH2,反应达到平衡时NH3的体积分数为20%,求此时的平衡常数________。
(5)合成塔从上到下将催化剂分成四层,在层与层之间冷激气(冷的原料气)和反应气混合,请问这样设计的原因是什么?_____________________________________下列有关工业生产的叙述正确的是 [ ] A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精炼铜时,同一时间内阳极溶液铜的质量比阴极析出铜的质量小下列是工业合成氨的简要流程示意图 
请回答下列间题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式:____________________,从冷凝器回流到压缩机中的X是_______。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因:______________。
(3)将N2、H2按体积比1:3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为___________________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因:__________________________。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途:__________________。实验室模拟合成氨和氨催化氧化的流程如下 
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从下图中选择制取气体的合适装置
氮气____________、氢气______________
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有___________、____________
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,______(填“会”或“不会”)发生倒吸,原因是 ___________________________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是_____________________,锥形瓶中还可观察到的现象是______________________。
(5)写出乙装置中氨氧化的化学方程式: __________________________。
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、__________、__________。合理设计工艺流程使资源最大化利用是目前解决资源匮乏问题的有效途径之一,如图表示某些化工生产的流程(有的反应条件和产物已略去)。 
请回答下列问题:
(1)写出上述流程中所涉及的化学工业名称______________
(2)反应I需在400~500℃下进行,其主要原因是______________;H转化为I的过程中,需不断补充空气,其原因是______________
(3)写出反应Ⅲ的化学方程式________________________
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通氨气的作用是
_________(填序号)。
a.增大NH4+的浓度,使J更多地析出 b.使K更多地析出 c.使K转化为M,提高析出的J的纯度(Ⅰ)在容积不变的密闭容器中,分别充入1.0mol N2和3.0molH2,任其发生反应:
N2(g)+3H2(g) 2NH3(g),分别在不同时测定NH3的含量,然后绘制出下图
2NH3(g),分别在不同时测定NH3的含量,然后绘制出下图
试回答下列问题:
(1)A、C段的曲线是增函数,C、E段曲线是减函数,试从反应速率和化学平衡的角度说明理由:
_____________________
(2)此可逆反应的正反应是________反应(填“放热”或“吸热”),在实际生产上,合成氨反应一般选择在500℃左右的温度下进行,试从化学平衡移动原理和综合因素等角度分析“选择在500℃左右下进行”的原因:____________________
(Ⅱ)利用天然气合成NH3的工艺流程如下
依据上述流程,完成下列填空:
(3)天然气脱硫时的化学反应方程式是___________________
(4)nmol甲烷经一次转化后产生CO 0.9nmol,则产生H2_________摩(用含n的代表式表示)。
(5)上述过程中包含了三个循环,一是Fe(OH)3循环,二是K2CO3循环,请在上述流程图中标出第三处循环(指出循环方向和循环物质)。2007年诺贝尔化学奖授予德国化学家GerhardErtl,以表彰他在表面化学领域研究所取得的开拓性成就。某反应在Pt/Al2O3/Ba催化剂表面吸附与解吸作用的机理如图所示(图中HC表示碳氢化合物,mtrate指硝酸盐),该机理研究是指 
[ ] A.汽车尾气催化转化处理
B.钢铁生锈机理
C.合成氨工业催化氧化机理
D.氢氧燃料电池电极反应机理氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②
4NH3 (g)+5O2(g) 4NO(g)+6H2O(g) △H= -905kJ/mol ①
4NO(g)+6H2O(g) △H= -905kJ/mol ①
4NH3 (g)+3O2(g) 2N2 (g)+6H2O(g) △H= -1268kJ/mol ②
2N2 (g)+6H2O(g) △H= -1268kJ/mol ②
下列说法正确的是[ ] A.工业上进行氨催化氧化生成NO时,温度应控制在780~840℃之间
B.工业上采用物料比n(O2)/n(NH3)在1.7~2.0,主要是为了提高反应速率
C.在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
D.氮气氧化为NO的热化学方程式为:N2(g)+O2(g) 2NO(g) △H =+181. 5kJ/mol
2NO(g) △H =+181. 5kJ/mol 我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出): 
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在T℃、pkPa时完全反应,生成一氧化碳和氢气(合成气),吸收了akJ的热量。该反应的热化学方程式是___。
(2)上述流程中,分离H2和CO2的合理方法是___(填序号)。
A.混合气先通入氢氧化钠溶液,再向溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆中,然后高温煅烧固体
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行____,目的是____ ;在合成氨的实际生产过程中,常将生成的氨从混合气体中分离出来,分离出氨的方法为____。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会和全人类负责的表现,请用线段和箭头画出图中两处合理利用资源的情况:___ 。利用天然气合成氨的工艺流程示意如下 
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是__________________。
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2________mol(用含n的代数式表示)
(3)K2CO3(aq)和CO2反应在加压下进行,加压的理论依据是_______(多选扣分)
(a)相似相溶原理 (b)勒沙特列原理(c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于________________(写出CO2的一种重要用途)
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)工业上的“三酸两碱”是指硫酸、硝酸、盐酸、纯碱和烧碱,氨气与这些工业原料的生产有密切关系。如氨气是生成硝酸、纯碱的原料,其水溶液是硫酸工业中尾气的吸收剂。部分生成工艺流程图或装置图如下:
材料一候氏制纯碱工艺流程图
气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱
材料二阳离子交换膜法电解饱和食盐水原理示意图
材料三某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备
(NH4)2SO4的工艺流程
根据以上材料,回答下列问题
(1)第Ⅳ步操作名称_______,为什么先通入A气体再通B气体?______________。
(2)材料二中精制的食盐水通过离子交换膜电解槽电解,透过阳离子交换膜的离子a是______;b入口通入的溶液是______________,电解饱和食盐水的离子方程式是_____________________。
(3)工业上除用电解法制烧碱外,还可用石灰--纯碱法来生产,写出有关反应方程式:_____________。
(4)材料三中的沉淀池内发生的主要反应方程是______________,从绿色化学和资源综合利用的角度说明上述流程的主要优点是__________________。氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
(1)已知:H-H键能为436 kJ/mol,N N键能为945 kJ/mol,N-H键能为391 kJ/mol。写出工业合成氨反应的化学方程式__________________;由键能计算说明此反应是______反应(填“吸热”或“放热”),合成氨反应(消耗1molN2时)的△H=_________。
(2)恒温下,向一个2L的密闭容器中充入1 mol N2和2.6 mol H2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示
5min内,用N2浓度的变化表示的反应速率为_________,此条件下该反应的化学平衡常数K=_________;反应达到平衡后,保持温度、容积不变,若向平衡体系中加入0.4 mol N2、1 mol H2和0.2 mol NH3,化学平衡将向_________方向移动(填“正反应”或“逆反应”)。
(3)氨是氮肥工业的重要原料。某化肥厂生产铵态氮肥(NH4)2SO4的工艺流程如下
① 向沉淀池中加入CaSO4悬浊液后,需先通入足量NH3,再通入CO2的原因是__________________。操作Ⅰ的名称是_________。
② 煅烧炉中产生的固态副产品为_________,生产流程中能被循环利用的物质X为_________。现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高。2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,氢气和氮气在电极上合成了氨,反应物转化率大大提高。请回答:
(1)哈伯合成氨的化学方程式为____________ ;在电解法合成氨的电解池中______(填“能”或“不能”)用水作电解质溶液的溶剂,原因是______________________ 。
(2)新法合成氨电解池中的电解质能传导H+,请写出阴极反应式___________。
(3)氨是一种重要的化工原料,在一定条件下氨可与其他物质反应生成化肥──尿素
〔 CO(NH2)2 〕。已知3.01×1022个尿素分子在高温、高压下分解生成0.85g NH3、0.56 L CO2(标准状况下)和一定数量的三聚氰胺分子。三聚氰胺的相对分子质量为126,则三聚氰胺的分子式为___________ ,尿素分解的化学反应方程式为______________ 。已知三个A分子可反应得到一分子三聚氰胺,请写出A的结构式_____________ 。下列反应起了氮的固定作用的是: [ ] A.氨经催化氧化生成NO
B.NO与O2反应生成NO2
C.N2在一定条件下与Mg反应生成Mg3N2
D.NH3与硝酸反应生成NH4NO3合成氨时采用500℃左右的温度进行,主要是因为在该温度时 [ ] A.合成氨的化学反应速率最大
B.N2的转化率最高
C.NH3在平衡混合气中的体积分数最大
D.催化剂的活性最大起固定氮作用的化学反应是 [ ] A.N2和H2在一定条件下反应生成NH3
B.NO与O2反应生成NO2
C.NH3催化氧化生成NO
D.由NH3制NH4HCO3和(NH4)2SO4将游离态的氮转化为化合态的氮的方法叫氮的固定。下列反应起氮的固定作用的是 [ ] A.N2与H2反应合成NH3
B.NH3经催化氧化生成NO
C.NO与O2反应生成NO2
D.由NH3制碳铵和硫铵某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程 
回答下列问题:
(1)沉淀池中发生主要反应的化学方程式为:_______________________ ,该反应能够发生的原因是:
_____________________。
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是:____________(填序号)。
A.萃取 B.蒸发浓缩 C.冷却结晶 D.蒸馏
(3)该生产过程中可以循环使用的物质X是:______________(填化学式)。
(4)上述生产流程中,有关NH3的作用及说明正确的是:_____________(填序号)。
A.提供制备所需的氮元素
B.增大CO32-的浓度促进反应发生
C.作反应的催化剂
D.生产1 mol (NH4)2SO4,至少消耗2 mol NH3氨广泛应用于工农业生产。
(1)工业合成氨的反应:N2(g)+3H2(g) 2NH3 ( g) △H = -a kJ . mol-1
2NH3 ( g) △H = -a kJ . mol-1
① 1/2N2(g)+3/2H2(g) NH3(g) △H = -b kJ . mol-1
NH3(g) △H = -b kJ . mol-1
② 反应①的化学平衡常数表达式为____,a与b的关系为___(用等式表示,下 同),若分别用m、n表示反应①、②的化学平衡常数,m与n的关系为___。
(2)氨的用途之一是制备氮肥,下列化肥属于复合肥料的是___。
A.碳酸氢铵 B.尿素 C.磷酸氢二铵 D.硝酸钾
(3)氨水是一些金属离子的常见沉淀剂。
①常温下,0.01 mol/L氨水的pH =10,则一水合氨的电离平衡常数为___。
②工业废水中常含有Cr2O72- ,其有剧毒,工业处理方法一般为加入还原剂(如亚铁盐)将其还原成+3价铬,再用氨水作沉淀剂使其沉淀。常温下,Cr(OH)3的溶度积Ksp=1×10-32,要使 c( Cr3+)降至10-5 mol/L以下,溶液的pH应调至___。有关合成氨工业的说法中,正确的是 [ ]
A.从合成塔出来的混合气体,其中NH3只占15%,所以生产氨的工厂的效率都很低
B.由于氨易液化,N2、H2在实际生产中是循环使用,所以总体来说氨的产率很高
C.合成氨工业的反应温度控制在500℃,目的是使化学平衡向正反应方向移动
D.合成氨厂采用的压强是2×107Pa~3×107Pa,因为该压强下铁触媒的活性最大合成氨工业中的主要反应是N2+3H2  2NH3(正反应为放热反应)。
2NH3(正反应为放热反应)。
(1)生产中,采用2×107Pa~3×107 Pa是为了_____________。
(2)加热到500℃,其目的是___________。
(3)使用催化剂是为了_____________。
(4)采用循环操作是为了_____________。
(5)若反应容器的体积不变,并维持原反应温度,而将平衡体系中的混合气体浓度增大一倍,则上述平衡向___________方向移动,原因是______________。
- 1阅读理解 It seems that fate likes to play strange jokes on t
- 2根据要求提取下面一段话的主要信息,写出四个关键词(可以是短语)。 由于司马迁认识到了历史终归是“人”的历史,不是“天”
- 3甲、乙两种固体纯净物的溶解度曲线如图A所示。在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解
- 4A hot dog is one of the most popular American food. It was n
- 5依次填人下列各句横线处的词语,最恰当的一组是 ①“绿色奥运志愿者林”建设活动实施3年来,已建设奥运志愿者林3处,--
- 6—Can I run around here?—______. Don’t you know the school ru
- 7采用地理信息技术,可以较快地监测植物虫害情况。下图反映的是不同健康状态松树的光反射情况。 1.对松树进行虫害监测可利用的
- 8书面表达(满分25分)假设你是某中学学生会主席李华,你校与本地一所国际学校经常举办联谊活动,你计划在重阳节组织学生到养老
- 9早点铺与星级酒店比较[ ]A.早点铺门槛人口少,服务范围小,数目多B.早点铺门槛人口多,服务范围大,数目少C.星
- 10______ has been said above, grammar is a set of dead rules.
- 1已知函数定义在R上的奇函数,当时,,给出下列命题:①当时, ②函数有2个零点③的解集为
- 239. Thank you for your help. ______ for your help, I wouldn’
- 3【题文】依次填入下面一段文字中方框处的关联词语,最恰当的一组是:( )□□不同的审美对象有不同的特
- 4常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关粒子的物质的量变化如图(
- 5某条约规定:“(一)从湖北省宜昌溯长江以至四川省重庆府。(二)从上海驶进吴淞口沿江及运河以至苏州府、杭州府。………臣民得
- 6李老师是某中学教师,他经常在自己的微博上评论政府工作,就政府决策提出自己的建议。李老师是通过A.社情民意反映制度参与民主
- 7阅读下面的材料,按要求作文。 古代春秋时期,子罕拒绝了一个宋国人向他献上的宝玉。他对献玉的人说:“我把不贪婪当作珍宝,
- 8我国要全面贯彻党的宗教工作基本方针,依法管理宗教事务,发挥宗教界人士和信教群众在促进经济发展和社会和谐中的积极作用。关于
- 9如图表示血液流经人体内,某器官前后四种物质相对含量的变化情况,由此可以判断该器官是( )A.小肠B.肺C.肾脏D.肝脏
- 10下列关于英、法、美三国资产阶级革命相同之处表述正确的是A.都是为了推翻封建王朝统治B.都曾建立过君主宪政体C.都由资产阶


 NO3-
NO3-  NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑  2NH3
2NH3