题目
题型:不详难度:来源:

请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为______;10min时,改变的外界条件可能是______.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)反应CO(g)+H2O(g)⇌CO2(g)+H2(g)800℃时,反应的化学平衡常数K=1.0.
①某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 | |||||||||||||||||
| 0.5mol | 8.5mol | 2.0mol | 2.0mol | |||||||||||||||||
| (1)由图可知,由图可知,在5~10分钟、12分钟后,甲烷浓度不变,是平衡状态;10min时甲烷的浓度继续减小,该反应向正反应方向移动,而该反应为吸热反应,则升高温度符合题意, 故答案为:5~10分钟、12分钟后;升高温度; (2)甲、乙两容器中分别充入等物质的量的CH4和CO2,且甲、乙两容器初始容积相等,由图可知,甲的体积不变,乙的压强不变,则假定甲不变,乙中发生CH4+CO2⇌2CO+2H2,其体积增大,则相当于压强减小,化学平衡向正反应方向移动,乙容器中CH4的转化率增大,但压强小,反应速率减慢,则达到平衡的时间变长,则乙中CH4的转化率随时间变化的图象为:  , ,故答案为:  ; ;(3)由表格中的数据可知,气体的体积相同,则物质的量与浓度成正比,Qc=
故答案为:a; ②800℃时,反应的化学平衡常数K=1.0,向体积为2L的密闭容器中充入2mol CO和4mol H2O,设参加反应的CO为xmol; CO(g)+H2O(g)⇌CO2(g)+H2(g) 起始量(mol):2 400 转化量(mol):x xx x 平衡量(mol):2-x 4-x xx K=
所以x=
所以平衡时CO的转化率为:
答:达到平衡时CO的转化率66.7%. | ||||||||||||||||||||
在一密闭容器中有如下反应:aX(g)+bY(g)⇌nW(g).某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: 其中,ω(W)表示W在反应混合物中的体积分数,t表示反应时间.当其它条件不变时,下列分析正确的是( )
|



 pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).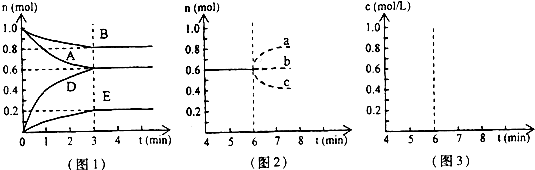
 CO(NH2)2+H2O,当氨碳比
CO(NH2)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如图所示,下列说法错误的是( )
,CO2的转化率随时间的变化关系如图所示,下列说法错误的是( )