百科
炔烃的性质
物理性质
炔烃的熔沸点低、密度小、难溶于水、易溶于有机溶剂,一般也随着分子中碳原子数的增加而发生递变。炔烃在水中的溶解度比烷烃、烯烃稍大。乙炔、丙炔、1-丁炔属弱极性,微溶于水,易溶于非极性溶液中碳架相同的炔烃,三键在链端极性较低。炔烃具有偶极矩,烷基支链多的炔烃较稳定。
化学性质
烷烃的化学性质:可发生氧化、取代、分解等反应。
烷烃的氧化反应:烷烃燃烧生成二氧化碳和水。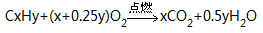
烷烃的取代反应:烷烃在光照下可发生取代反应。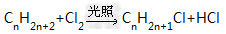
烷烃的分解反应:烷烃在高温条件下能够裂解。如: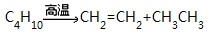
相关试题
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应。由此可以断定原气态烃是(气体体积均在相同条件下测定) [ ] A.乙炔
B.丙炔
C.丁炔
D.丁二烯当1 mol某气态烃与2 mol Cl2发生加成反应时,分子中的不饱和碳原子全部转化为饱和碳原子。所得产物再与2 mol Cl2进行取代反应后,此时原气态烃分子中的H原子全部被Cl原子所替换,生成只含C、Cl两种元素的化合物。该气态烃是 [ ] A.乙烯
B.乙炔
C.丙烯
D.丙炔x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下V L的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比可能是 [ ] A.1∶1∶1
B.1∶2∶3
C.1∶4∶1
D.3∶2∶1有机物键线式结构的特点是以线示键,每个折点和线端点处表示有一个碳原子,并以氢补足四价,C、H不表示出来。降冰片烷立体结构如图所示 
(1)写出其分子式__________,其分子式符合__________烃的通式,请你写出一种这种烃类物质的结构简式 _______________。
(2)当降冰片烷发生一氯取代时,能生成________种沸点不同的产物。
(3)结合降冰片烷及其键线式,请你判断:降冰片烷属于________。
a.环烷烃 b.饱和烃 c.不饱和烃 d.芳香烃
(4)降冰片烷具有的性质是__________。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体 e.能发生取代反应1mol气态烃A最多和2mol HCl加成,生成氯代烷B,1mol B与6mol Cl2发生取代反应,生成只含碳、氯两种元素的化合物。则A的分子式为 [ ] A.C2H2
B.C3H4
C.C3H6
D.C4H6某烃1 mol最多能和2 mol HCl加成,生成氯代烃,此氯代烃l mol能和6 mol Cl2发生取代反应,生成物中只有碳氯两种元素,此烃为 [ ] A.C2H2
B.C2H4
C.C3H4
D.C6H6与氢气完全加成后,不可能生成2,2,3-三甲基戊烷的烃是 [ ] A.CH2=C(CH2CH3)C (CH3)3
B.CH2=C(CH3)C(CH3)2CH2CH3
C.HC≡CCH(CH3)C(CH3)3
D.(CH3)3CC(CH3)=CHCH3据报道,近来发现了一种新的星际分子氰基辛炔,其结构简式为:HC≡C-C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是 [ ] A.晶体的硬度与金刚石相当
B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应
D.可由乙炔和含氮化合物加聚制得关于炔烃的说法,不正确的是 [ ] A.相同碳原子数的炔烃与二烯烃是同分异构体
B.易发生加成反应
C.既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
D.分子里所有的碳原子都处在同一条直线上下面有关丙烷、丙烯、丙炔说法正确的是 [ ] A.如图所示,丙烷、丙烯、丙炔的球棍模型分别为 
B.相同物质的量的3种物质完全燃烧,生成的气体在标准状况下,体积比3:2:1
C.相同质量的3种物质完全燃烧,丙烷消耗的氧气最多
D.丙烷的一氯代物只有1种如图所示是由4个碳原子结合成的4种有机物(氢原子没有画出) 
(1)写出有机物(a)、(b)的系统命名法的名称:___________________。
(2)写出有机物(a)的同分异构体的结构简式:________________。
(3)上述4种有机物中,互为同分异构体的是_______________ (填代号),存在顺反异构体的有机物是________________ (填代号)。
(4)上述4种有机物中,既能使酸性KMnO4溶液褪色,又能使澳水褪色的有机物是_________(填代号);(a)可与 Cl2发生______________反应(填反应类型)生成_______________种一氯代物。
(5)上述有机物中4个碳原子处于同一平面的有____________(填代号)。有下列八种不饱和烃: A: CH2=CH-CH=CH2 B:  C:CH2=CH-CH=CH2-CH3 D:
C:CH2=CH-CH=CH2-CH3 D: 
E: F: CH
F: CH CH G: CH3-C
CH G: CH3-C CH H: CH3-C
CH H: CH3-C C-CH3
C-CH3(1)已知A+F  若要合成则下列所选原料正确的是_________
若要合成则下列所选原料正确的是_________
①D和H ②E和H ③E和F ④B和H ⑤C和H ⑥D和G
(2)A和Br2的CCl4溶液发生反应时,可生成多种产物,写出这些产物的结构简式:
________、________、________、________。乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。 
完成下列各题:
(1)正四面体烷的分子式为___________,其二氯取代产物有__________种。
(2)关于乙烯基乙炔分子的说法错误的是__________
a.能使酸性KMnO4溶液褪色
b.1 mol乙烯基乙炔能与3 mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式: ______________ 。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例): ________ 、__________。据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为: HC≡C-C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是 [ ] A.晶体的硬度与金刚石相当
B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应
D.可由乙炔和含氮化合物加聚制得下面有关丙烷、丙烯、丙炔说法中正确的是 [ ] A.如图,丙烷、丙烯、丙炔的结构分别表示为 
B.相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1
C.丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大
D.丙烷的碳原子空间结构呈线性排列某气态烃0.5mol能与1molHCl完全加成,加成后产物分子上的氢原子又可被3molCl2恰好完全取代,则此气态烃可能是 [ ] A.CH≡CH
B.CH2=CH2
C.CH≡C-CH3
D.CH2=C(CH3)2据报道,近来发现了一种新的星际分子氰基辛炔,其结构简式为:HC≡C-C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是 [ ] A.其分子中的原子都在一条直线上
B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应
D.可由乙炔和含氮化合物加聚制得据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C—C≡C-C≡C-C≡C-C≡N。对该物质判断正确的是 [ ] A.晶体的硬度与金刚石相当
B.能使酸性高锰酸钾溶液褪色
C.不能发生加成反应
D.可由乙炔和含氮化合物加聚制得关于炔烃的描述中不正确的是 [ ] A.分子含有碳碳三键的不饱和链烃
B.易发生加成反应,也易发生取代反应
C.既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
D.分子里所有的碳原子都处在同一直线上某气态烃0.5mol恰好与1molHCl加成,生成物中的氢又可被3molCl2取代,则此气态烃可能是 [ ] A.C2H2
B.C2H4
C.CH≡C-CH3
D.CH2=C(CH3)2某气态烃1 mol最多和2 mol氢气发生加成反应,所得产物又能与10 mol氯气发生取代反应,最后得到一种只含碳、氯元素的化合物,则原气态烃为 [ ] A. 2-辛炔
B. 丙烯
C. 2-丁炔
D. 2-戊炔(1)若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为____________________________________________。
(2)分子式为C9H20的某烃其一氯代物只有两种产物,写出符合要求的结构简式_____________________________________
(3)分子式为C5H10的烯烃中不存在顺反异构的物质有_____种
(4)分子式为C5H12O2的二元醇有多种同分异构体,其中能够氧化成主链上碳原子数为3的二元醛有_______种
(5)已知烯烃、炔烃在臭氧作用下发生以下反应:
某烃化学式为C10H10,在臭氧作用下发生反应:
C10H10 H2OCH3COOH+3HOOC-CHO+CH3CHO
H2OCH3COOH+3HOOC-CHO+CH3CHO
①C10H10分子中含________个双键,________个三键。
②C10H10结构简式为____________________________。已知某炔烃与卤素按物质的量为1:2发生加成反应后,生成的有机物至少需6mol的卤素单质才能把生成的有机物中的氢全部取代,则该炔烃可能是 [ ] A.丙炔
B.1-丁炔
C.3-己炔
D.2-庚炔现有分子式为CnHmO2的某有机物,1 mol该有机物在氧气中完全燃烧后,产生等物质的量的CO2和H2O,并消耗78.4 L(标准状况)氧气,该有机物分子中碳原子数n是( ) A.2 B.3 C.4 D.5 钠与下列物质均能反应产生氢气:①H2O;②CH3COOH;③CH3CH2OH。试根据所学知识推断这三种物质电离出H+从难到易的顺序为( ) A.①②③ B.②③① C.③①② D.②①③ 将一定量的某有机物与过量的钠反应,生成H2V1 L;另取等量的该有机物与足量Na2CO3溶液反应生成CO2V2 L(同条件下),则V1和V2的关系不可能为( ) A.V1<V2 B.V1=V2 C.V1>V2 D.V1=2V2 中学有机化学中同学常碰到关于乙醛和溴反应的问题,对此同学常有如下不同的观点:
①乙醛中醛基有强还原性,而溴单质(Br2)有强氧化性,因而两者可发生氧化还原反应。
②乙醛分子中羰基含有碳氧双键,因而可和Br2发生加成反应。
③乙醛分子中的烃基可和溴发生取代反应。
为此,某同学进行如下实验,并记录了相关实验事实:
实验1:在1mL Br2的CCl4溶液中加入1mL乙醛,发现溶液分层,下层橙黄色,上层无色溶液无明显现象。
实验2:在1mL饱和的溴水中加入1mL乙醛,振荡试管后静置,发现溶液不分层,且发现溴水褪色。
1.根据以上实验1,2及相关实验事实,请你对乙醛和溴的反应原理作出相应的分析:
(1)根据实验1,可推知
(2)根据实验2,可推知
2.目前有一个较为典型的试题是:
“已知柠檬醛的结构简式为(CH3)2C=CHCH2CH2CH=CHCHO,如何检验出其中的C=C双键?”通常的实验方法是:“先加足量的银氨溶液[或新制的Cu(OH)2],取上层清液加酸中和后,然后再用酸性KMnO4溶液(或溴水)检验C=C双键。”
(1)请分析该实验检验方法是否合理 ,为什么?
(2)根据以上提供的实验事实,是否有更为简便的检验方法? ;如果有,请简单说明该实验方法 ;如果没有,则不必说明。[江苏省南通中学2008学年度第一学期期末复习高三化学 ].某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙、丙三套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。 
(1)简述两套方案各自的优点:甲:_________________、_________________________,
乙:___________________
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为________________(例如甲①,乙②)
(3)若要保证此实验有较高的效率,还需补充的仪器有__________。理由______。
(4)实验中能验证乙醇氧化产物的实验现象是_______________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式____________。下列叙述:①我国科学家在世界上第一次人工合成结晶牛胰岛素;②最早发现电子的是英国科学家道尔顿;③测定有机化合物中碳、氢元素质量分数的方法最早由李比希提出;④荷兰化学家范特霍夫提出碳原子成键的新解释,成功地解决了二取代甲烷只有一种结构的问题;⑤首先在实验室合成尿素的是维勒,其中正确的是( ) A.只有① B.①和③ C.①②③⑤ D.①③④⑤ 某有机物含碳40%、含氢6.67%、含氧53.3%,如果0.2mol该有机物的质量为 6g , 则它的化学式为( )。 A.C2H2O2 B.C2H4O C.CH2O D.C2H4O2 TBC是优良的增塑剂,具有很好的相容性,且挥发性小、耐寒、耐光及耐水等,广泛用于医学卫生用品,它的结构式如右图,合成时柠檬酸与正丁醇合成数据如下: 

下表中实验数据均为用活性炭固体杂多酸作催化剂,实验时催化剂总量占原料的1%,实验结果如下表。表1:酸醇物质的量之比对酯化率的影响;表2:酯化时间对酯化率的影响;表3:酯化率随温度变化情况。表1 n(酸)︰n(醇) 1︰5.0 1︰5.5 1︰6.0 1︰6.5 1︰7.0 酯化率/% 95.1 96.3 97.0 97.4 97.2 表2 时间/h 0.5 1.0 2.0 3.0 5.0 酯化率/% 40.0 70.2 94.3 97.4 97.4 表3 温度/℃ 130 140 145 150 160 酯化率/% 89.5 96.2 97.4 97.4 97.2
试回答下列问题
(1)酯化反应适宜的条件n(酸)∶(醇)、时间/h、温度/℃分别是: ▲ (选填序号)。
A.1∶5,1,130 B.1∶5.5 ,1,140
C.1∶7 ,2,160 D.1∶6.5 ,3,145
(2)TBC的一种标准谱图如右,它是 ▲ (A、1H-NMR图谱 B、红外光谱 C、质谱)
(3)TBC与足量NaOH溶液反应的化学方程式: ▲ 。
(4)柠檬酸的一种同分异构体A,能发生如下转化:
A可能的结构式为: ▲ (只写一种)。实验测得某碳氢化合物A中,含碳80%、含氢20%,求该化合物的实验式。又测得该化合物的相对分子质量是30,求该化合物的分子式。 2.3g某有机物A完全燃烧后,生成0.1 mol CO2和 2.7gH2O,测得该化合物的蒸气与空气的相对密度是1.6,求该化合物的分子式。 某烃含碳氢两元素的质量比为3∶1,该烃对H2的相对密度为8,试确定该烃的分子式.
某酯A的化学式为C9H10O2,且A分子中只含有1个苯环,苯环上只有一个取代基。现测出A的1H-NMR谱图有5个峰,其面积之比为1︰2︰2︰2︰3。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得A分子的红外光谱如下图: 
、
试回答下列问题。
(1)A的结构简式可为C6H5COOCH2CH3 C6H5CH2OOCCCH3、 。
(2)A的芳香类同分异构体有多种,请按要求写出其中不含甲基且属于芳香酸的B的结构简式: 。
(3)已知C是A的同分异构体,分子中不含甲基,且遇FeCl3溶液显紫色,苯环上只有两个对位取代基的芳香醛,且有如下转化关系。
 ① 写出D E的化学方程式 。
① 写出D E的化学方程式 。
② 请用合成反应流程图表示出由C合成F的最合理的合成方案(注明反应条件)。
 提示:合成反应流程图表示方法示例如下:
提示:合成反应流程图表示方法示例如下:
测定有机物相对分子质量常用的物理方法是 ( ) A.质谱法 B.红外光谱法 C.紫外光谱法 D.核磁共振谱法 下列各组物质,分别取等物质的量,在足量氧气中完全燃烧,消耗氧气量不同的是 A.乙炔和乙醛 B.乙烯和乙醇 C.乙酸和乙醇 D.乙酸和甲酸甲酯 等质量的下列烃,分别完全燃烧时,消耗氧气的量最多的是 A.甲烷 B.乙烯 C.苯 D.甲苯 未知物A的实验式和分子式都是C2H6O。A的红外光谱图如图(a),未知物A的核磁共振氢谱有三个峰如图(b),峰面积之比是1∶2∶3,未知物A的结构简式为____________。 
在真空中,用高能电子轰击一种气体分子时,分子中的一个电子可以被轰击出去,生成阳离子自由基。如苯甲酸分子被轰击:
C6H5COOH® C6H5COOH++e
其阳离子的式量与所带电荷数之比( )为122(即
)为122(即 ),与此同时,这样的离子还会被轰击成其它形式的碎片离子(都只带一个单位的正电荷)。各有它们的
),与此同时,这样的离子还会被轰击成其它形式的碎片离子(都只带一个单位的正电荷)。各有它们的 ;由苯甲酸形成的碎片离子按所测得的
;由苯甲酸形成的碎片离子按所测得的 大小排列有:122、105、77、51……。
大小排列有:122、105、77、51……。
碎片离子 有关反应 105 C6H5CO+ C6H5COOH+® C6H5CO++OH 77 C6H5+ C6H5CO+® C6H5++CO 51 C4H3+ C6H5+®C4H3++C2H2 …… …… ……
现有中学常用的有机化合物A,仅由C、H、O元素组成,通常A是一种无色透明的液体,不溶于水,加热后能逐渐溶于稀NaOH溶液或稀H2SO4溶液,冷却后不再析出原有的液体。若用高能电子束轰击气体A分子时,在70eV下可得 为88、73、61、45、29、27、15等的离子(均只带一个正电荷)。回答下列问题:
为88、73、61、45、29、27、15等的离子(均只带一个正电荷)。回答下列问题:
(1)有机物A的相对分子质量是 ,分子式是 ;
(2) 为88的离子是 ;
为88的离子是 ;
(3) 为15的离子是 。
为15的离子是 。蛋白质是一类复杂的含氮化合物,每种蛋白质都有恒定的含氮量(约在14%-18%,质量分数),食品中蛋白质的含量测定常用凯氏定氮法。其测定原理是:
I.蛋白质中的氮在强热和CuSO4、浓硫酸作用下,生成一种无机含氮化合物(NH4)2SO4;
II. (NH4)2SO4在凯氏定氮测定器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7;
III.用已知浓度的HCl标准溶液滴定,根据消耗的HCl量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%。不法分子通过在低蛋白含量的奶粉中加入三聚氰胺来提高奶粉中蛋白质的含量,导致许多婴幼儿患肾结石。三聚氰胺的结构如下:
①三聚氰胺的分子式为 ,其中氮元素的质量分数为 。
②下列关于三聚氰胺的说法中,正确的有 。
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的奶粉中掺入多少克三聚氰胺即可使奶粉检测“达标”?A.三聚氰胺中只含有碳、氢、氮三种元素 B.三聚氰胺中含有苯环结构,属于苯的同系物 C.三聚氰胺不是组成蛋白质的成分 D.三聚氰胺为高分子化合物 下列反应属于取代反应的是 。
①CH2=CH2+HCl→CH3CH2Cl ②Fe+2HCl=FeCl2+H2↑③CH4+Cl2 CH3Cl+HCl
CH3Cl+HCl
④ ⑤CH3COOH+CH3CH2OH
⑤CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O下列物质能使酸性高锰酸钾溶液褪色的是( ) A.甲烷 B.乙烷 C.乙烯 D.苯
最新试题
- 1根据家兔和狼的牙齿图解,回答下列问题:(1)图中有磨碎食物作用的是[ ]________。(2)图_______
- 2在矩形ABCD中,AB=2,AD=3,∠DAB和∠ABC的平分线交于点O,连结OC,OD,将矩形分成四等分,四部分的面积
- 31854年,英国外交大臣致函英国驻华公使说:“为了适应外商对农业产品已增加的需要,……新的贸易市场尚待进行。”l856年
- 4对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )①Zn是负极 ②电子由Zn经外电路流向
- 5The school has very strict rules about cheating in exams, so
- 6请你写一个能先提公因式,再运用公式来分解因式的三项式,并写出分解因式的结果( )(答案不唯一)
- 7下列加粗词语使用不当的一项是[ ]A、虽然攀枝花与汶川地震灾区相隔遥远,但我们的心和灾区人民的心是息息相通的。B
- 8While traveling, whether on business or for _____ , you ofte
- 9—What"s this? —It"s a _____. [ ]A. egg
- 10已知,则的值为( )A.B.C.D.
热门考点
- 1铝合金已成为许多现代家庭封闭阳台的首选材料,它具有轻巧、坚固、易于加工等优点,这与铝合金的下列物理性质无关的是( )A
- 2如图,正方形MNPQ网格中,每个小方格的边长都相等,正方形ABCD的顶点在正方形MNPQ的4条边的小方格顶点上。(1)设
- 3Morning is extremely important, because it is the beginning
- 4盐的水溶液不一定都呈中性,如NaHCO3溶液呈碱性.下列有关实验中,能够证明NaHCO3溶液呈碱性的实验事实是( )A
- 52010年我国西南地区发生严重的旱灾,期间某部队用装有碘化银(化学式为AgI)实施人工降雨,碘化银中碘元素的化合价为 [
- 6阅读下面的文字,完成问题。跟陌生人说话 刘心武 父亲总是嘱咐子女们不要跟陌生人说话,尤其是在公共场所。母亲对父亲给予子
- 7用大小不同的力敲音叉,发声的______(选填“响度”或“音调”)不同.敲击后,音叉的声音会逐渐变弱,则是因为音叉的__
- 8某建筑工地急需长12cm和17cm两种规格的金属线材,现工地上只有长为100cm的金属线材,要把一根这种金属线材截成12
- 9下列各句中没有语病的一句是A.巴金的“激流”三部曲等作品,不但反映出时代的风云变幻、人物的命运沉浮,更激励无数青年反抗封
- 10She _____ as the first lady of Republic of Korea instead of

 )
)  )
)  )
)  ,符合这一条件的炔烃有
,符合这一条件的炔烃有 


